Az új, hármas kombinációjú CFTR modulátor (Trikafta) amerikai engedélyeztetése után, a Vertex a 2019-es év végén kezdeményezte a gyógyszer gyorsított eljárású engedélyeztetését az Európai Gyógyszerügynökségnél (EMA), mely az ígéret szerint kb 2020 őszére megkapta volna így az európai forgalmazási engedélyt.
Az EMA azonban, eltérően az amerikai engedélyezési gyakorlattól, elsősorban klinikai vizsgálati eredményeken alapuló evidenciákat tekint elfogadhatónak. A Trikafta tesztelése során azonban a Vertexnek néhány ritka mutáció esetében, a rendkívül alacsony betegszám miatt nem volt lehetősége a készítmény hatékonyságát ilyen jellegű klinikai kísérletekkel igazolni.
Ilyen esetekben tehát a készítmény gyakorlatban bekövetkezett kedvező hatását nem tudják dokumentált klinikai eredményekkel alátámasztani, és ezt kifogásként emelte az EMA az engedélyezés során, illetve erre való hivatkozással az Európai Gyógyszerügynökség vissza is küldte további kérdések megválaszolására a Vertex számára. Ez azt is jelenti, hogy a Trikafta jelenleg lekerült a kiemelt gyorsasággal engedélyezendő termékek köréből
Az Európai CF szervezet (CFE), aggodalmát fejezte ki azért, mert ha a Vertexnek nem sikerül kielégítő válasszal illetve alátámasztott adatokkal igazolnia a készítmény hatásosságát a ritka mutációk esetében, úgy ezekre a mutációkra az EMA esetlegesen nem ad forgalombahozatali engedélyt, ami azt jelentené hogy bizonyos betegek nem kaphatják meg a Trikaftát Európában semmilyen felhasználásra.
Aggodalmaiknak hangot adva, fogalmazódottt meg az alábbi levél, amely továbbítva is lett az EMA vezetősége számára, 48 európai CF szervezet aláírásával és támogatásával:
Kedves Dr. Enzmann!
A CF Europe, egy 48 európai nemzeti CF egyesületet magában tömörítő szövetség nevében írok, ami az európai cisztás fibrózisos embereket és családjaikat képviseli.
EMA – Európai Gyógyszerügynökség ( European Medicines Agency )
CFE – CF Europa
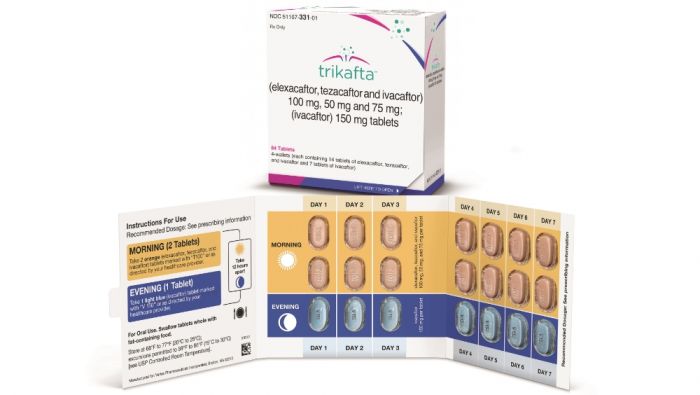
A cisztás fibrózisos (CF) közösséget világszerte lázba hozta a hármas kombinált gyógyszerről – Elexacaftor, Tezacaftorral és Ivacaftorral – szóló tanulmányok eredményei, mint egyértelmű előrelépés a CF leküzdésére irányuló átfogó küldetésünkben.
A kombinált készítmény két, döntő fontosságú, 3. fázisú kísérletének eredményei példátlan mértékű javulást mutattak a célcsoportban. Az egyértelmű, hogy a hármas kombinációjú gyógyszer hatékonysága felülmúlja az eddigi, kombinált készítményekét. Az Ivacaftor egyedüli alkalmazását tekintették referenciaként a magas hatásfokú modulátor készítményeknél, a legalább egy “érintett” mutációjú egyének esetében. Az ilyen mutációk a CF betegek mindössze 5%-át érintik világ- és Európa-szerte.
A hármas hatóanyagú gyógyszer klinikai kísérleteinek eredményei hasonló mértékű javulások lehetőségét mutatják egy sokkal gyakoribb mutációval. Ennek a jelentősége, hogy az Európai CF betegek, több mint 80%-ának van egy olyan genotípusa, amely kezelhető egy ilyen életminőséget javító, magas hatékonyságú gyógyszerrel.
Az Európai CF közösség számára, amikor várhatóan az EMA az év későbbi részében engedélyezi a gyógyszert, a következő nagy mérföldkövet jelenti , hogy a CF-esek többsége számára elérhetővé válik a hozzáférés ehhez a nagy hatékonyságú, új gyógyszerhez vezető úton.
A közösségi médiák korában, a kezelésben már részesült CF-esek bizonysága messzire jutott, ami fokozza az izgatottságot és reményt ad.
Természetesen, a CF-esek, akik kaphatják a gyógyszert és családjaik már nagyon bizakodóak, hogy kipróbálhatják, és – a progresszív állapotuk fényében és régóta tartó várakozás miatt – a szükséges engedélyezési folyamatok kivárása gyötrelmes és nehéz.
Ezért arra kérjük az Ügynökség döntéshozóit, hogy legyen szívesek a készítményt gyorsított eljárásban részesíteni.
A gyógyszer hozzáférhetőségének sürgősségét nehéz túlbecsülni. Az esetleírások azt mutatják, hogy a gyógyszer lényegesen képes javítani a végstádiumú CF betegek egészségi állapotát és életminőségét. Ez az akut eredmény, amit egy viszonylag jobb állapotban lévő csoporton bizonyítottak egy 3. fázisú kísérletben, hozzáadódik a betegség progressziójához kapcsolódó egészségügyi hatások csökkentéséhez, amiket megfigyeltek a kísérletekben.
Az ilyen hatások elkerülése halmozott eredményeket hozhat az évek alatt, hasonlóan az ivacaftor önálló alkalmazásában megfigyeltekhez. Hosszú idejű klinikai és valós használati adatok azt mutatják, hogy az ivacaftor tartósan hatásos az azt szedők körében, a légzésfunkció javításától és a fertőzések csökkentésétől, a tápláltság javításáig, ami a CF-esek számára, hosszabb, jobb minőségű életet adhat. Jelenleg figyelemre méltó ígéret, hogy ez a hármas kombinált készítmény sokkal több CF-esnek biztosíthatja ezt a minőségi javulást.
Miközben néhány klinikai kísérlet még mindig zajlik, általánosan elfogadott, hogy a jelenleg hivatalos technológiákkal és folyamatokkal nem megvalósítható a hatások alapos klinikai vizsgálata minden mutáció kombinációval. Azért aggódunk, hogy azok a CF-esek, akiknek a CFTR gén mutációja egy Delta-F508 és egy ritka mutációból áll, melyekre nincsenek jelenleg klinikai eredmények, kizáródnak a Marketing Authorisation most készülő tényleges orvosi javallatából.
Ennek tükrében kérjük, hogy kellő figyelmet biztosítsanak annak, hogy az orvosi javallatból ne kerüljenek véletlenül kizárásra azok, akiknek hatásos lehet a gyógyszer az egy Delta-F508 mutációjukon keresztül, annak következményében, hogy egy ritka mutációjuk is van. A jelenlegi kísérleti eredmények a hármas kombinációval azt az elméletet látszanak erősen alátámasztani, hogy egyetlen Delta-F508 allél megléte elegendő, hogy a terápia hatásos legyen. Ezért erősen hisszük azt, hogy a gyógyszer Európai engedélye ezt az érzést fogja tükrözni. Tisztelettel megköszönjük, amennyiben leírják az álláspontjukat a kérdéssel kapcsolatban.
Szeretnénk közösségünk támogatásának biztosítását megmutatni Önnek, beleértve a CF-es emberek és családtagjaik, az egészségügyi szakemberek és kutatók szakértelmét szerte Európából, és reméljük, hogy hasznosítani tudják az ő nézőpontjaikat munkájukban és döntésükben.
Üdvözlettel
Jacquelien J. Noordhoek MA MSc
Elnök
CF Europe
Fordította: Gulyás Gábor



Comments are closed.